化學家,為了能準確判斷一個化學反應的真實狀態,會仔細比較分子的化學鍵鍵能,在化學反應前後有什麼不同。
1. 許多人喜歡預測未來的事情,或從一個表面的現象去分析背後的真實狀態,這須要科學的訓練才能做到。化學家,為了能準確判斷一個化學反應的真實狀態,會仔細比較分子的化學鍵鍵能,在化學反應前後有什麼不同。
2. 「碳-氫」化學鍵的鍵能怎麼算呢?那就找由4個「碳-氫」化學鍵組成的甲烷,把它的化學鍵打斷成碳原子與氫原子,看釋放多少能量,所釋放的能量除以4,就是每個化學鍵的鍵能。
CH4→C+4H 甲烷→變成→1個碳+4個氫
「C-H」化學鍵: ΔH°/4 = 99kcal/mole
「碳-氫」化學鍵:熱能變化÷4 = 99千卡/每莫耳
3. 「碳-碳」化學鍵的鍵能怎麼算呢?乙烷,就是由1個「碳-碳」化學鍵骨架,和6個「碳-氫」化學鍵組成的,所以,先測量碳原子與氫原子形成乙烷所需的熱量,然後再扣除乙烷6個「碳-氫」化學鍵,就可以得到「碳-碳」化學鍵的鍵能。
2C+3H→C2H6 2個碳+3個氫→變成→乙烷
「C-C」化學鍵: ΔH° – 6×「C-H bond energy」= 83kcal/mole
「碳-碳」化學鍵:熱能變化– 6個「碳-氫鍵能」= 83千卡/每莫耳
4. 我們要注意一點,「碳-碳」、「碳-氫」化學鍵的鍵能,並不是固定的數值,不同的分子,鍵能常常不一樣。
5. 化學世界的分子非常多樣,光「碳-碳」化學鍵就至少可分為單鍵、雙鍵、三鍵;「三鍵」的鍵能,大於「雙鍵」的鍵能,「雙鍵」的鍵能大於「單鍵」的鍵能。
6. 「碳-氫」化學鍵容易受相鄰原子或化學鍵的影響,如果靠近鍵能較強的「碳-碳雙鍵」,「碳-氫」化學鍵的鍵能會變強。
7. 鹵素族群原子,都有是負電性強的原子,但是強度不一樣。負電性由強而弱:氟F > 氯Cl> 溴Br> 碘I,所以,「氫-鹵素 H-X」化學鍵強度是:「氫-氟H-F」>「氫-氯H-Cl」>「氫-溴H-Br」>「氫-碘H-I」。
8. 化學鍵對分子有什麼影響呢?思考這類問題,就好像在問一個土木技師,建築的鋼骨結構,對整棟建築物有什麼影響呢?
9. 由木頭為梁柱的傳統廟宇和鋼骨結構的現代高樓相比,我們一定認為現代高樓比較安穩,因為鋼骨強度、耐受度都比木頭好得多;同樣的道理,也發生在有機化學的世界。
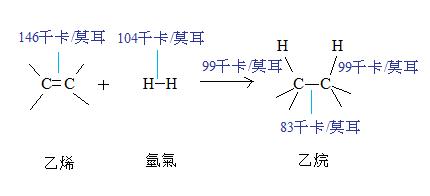
10. 乙烯ethene和氫氣結合成乙烷ethane,乙烯的「C=C 碳-碳雙鍵」與氫氣的「H-H 氫-氫單鍵」被打斷,轉換為乙烷的「C-C碳-碳單鍵」,和2個「C-H 碳-氫單鍵」。
11. 化學變化前,乙烯「C=C」與氫氣「H-H」的化學鍵總鍵能250千卡/莫耳;化學變化後,乙烷的「C-C」和2個「C-H」總鍵能是281千卡/莫耳,化學鍵的總鍵能增加了,這代表什麼意思?分子的穩定度增加。
12. 就像有些高樓,會讓它的鋼骨有彈性又堅韌,好提高抗震、抗風的能力;同樣地,烷類分子的化學鍵,跟烯類分子相比,比較有彈性、可以自由轉動,比較耐得住其它分子的碰撞,結構不會被破壞。
13. 人類習慣透過實驗來了解分子的能量,實驗的經驗顯示,散熱之後,分子會變得比較穩定,「散熱」這件事讓人類感覺能量變少了,所以人類認為,比較穩定的分子,能量比較低,這是目前化學、有機化學教科書的觀點。
14. 這個看法有以下幾點侷限:1. 分子的能量可以分為內外兩部分,內部就是它的化學鍵強度,外部就是它的穩定度。穩定度提高的時候,人類認為分子能量降低,可是,實際上分子內部的化學鍵鍵能增加。
15. 2. 「散熱」不一定是能量減少。如果我們把一塊地面上的大石頭,從平地拖拉上坡500公尺,過程中石頭與地面的阻力互相「摩擦」而散熱,但最後石頭的位能卻增加了,也就是說,如果有人想把山坡上500公尺的大石頭往下推,站在下方的人鐵定會被它滾落的力道打傷,雖然它曾經散熱「散熱」。
16. 3.化學鍵的鍵能,是透過打斷化學鍵的實驗來測量。所以,比較化學前後分子化學鍵的鍵能,其實是比較他們的「散熱」,也就是分子被破壞的熱含量變化。
17. 把散熱用負號「–」象徵,乙烯加氫反應的熱含量變化(焓變化),就是:
(乙烯的化學鍵鍵能)+ (氫氣的化學鍵鍵能)–(乙烷的化學鍵鍵能) 也就是
(–乙烯焓變化)+ (–氫氣焓變化)–(–乙烷焓變化) 也就是
(–乙烯和氫氣的焓變化) – (–乙烷焓變化) 負負得正,就是
(–乙烯和氫氣的焓變化) + 乙烷焓變化 意思就是
乙烯和氫氣的散熱 和 乙烷的吸熱 二者相比
如果 散熱比吸熱多,那整個化學反應過程就是散熱,結果會是負數(–);如果散熱比吸熱少,那整個化學反應過程吸熱,結果會是正數。
ΔH° = + 146 + 104 –83 – (2×99) = –31千卡/莫耳
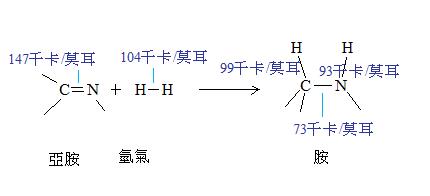
18. 同樣地,我們也可以用同樣的思考邏輯,計算亞胺的加氫反應。化學鍵互相比較的結果是散熱14千卡/莫耳。
ΔH° = + 147 + 104 –99 – 93 – 73= –14千卡/莫耳
19. 「散熱,就是某種能量物質從分子流失,使得分子的能量下降」,這個觀念很像十八世紀以前盛行的《燃素說》:「物質含有燃素,物質燃燒之後變得比較輕,是因為它的燃素跑出來、被燒掉了」。
20. 推翻《燃素說》的拉瓦錫認為,物質燃燒是因為它們與「氧」結合,跟物質跑出什麼燃素無關,化學反應前後質量一樣,只是排列順序不同,有些物質化學反應之後讓人類感覺變輕,是因為一部分的原子重新排列後變成氣體分子,跑到空氣中了。這就是著名的「氧化還原」理論。
21. 我們的思考難已突破,常常是因為依循慣性的框架。拉瓦錫打破「固體物質永遠是固體」的框架,提出質量不滅,指出物質可能在固體、液體、氣體這三種狀態中變化,因此發展出現代化學。
22. 乙烯和氫氣作用變成乙烷,雖然是散熱,但是反應之後,化學鍵的總鍵能變強,顯然分子內部的能量增強,所以,不是教科書圖示的分子能量下降,而是能量上升;散熱,應該只是分子重組時,原子與周遭粒子或相鄰原子碰撞摩擦生熱。
23.