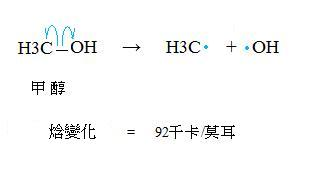
1. 從一個穩定的有機分子,變為另一種分子的轉變過程中,不可避免地會伴隨化學鍵「鍵結」的改變,現有化學鍵被打斷,新的化學鍵形成。打斷化學鍵是需要耗費能量的。
2. 均勻斷裂Homolytic cleavage:原本互相鍵結的二個原子,化學鍵被打斷,電子平均分配到二個獨立的原子身上;打斷化學鍵需要耗費的能量,就是鍵解離能bond dissociation energy。
3. 均勻斷裂會產生2個自由基radical。什麼是自由基?鍵結時二個原子互享電子,使彼此的外圍電子都填滿,進入穩定狀態,打斷之後,彼此電子不再共享,這使得每個原子的外層電子無法填滿,都少一個電子,這種欠缺1個電子的狀態,就叫自由基。
4. 舉例來說,甲醇的碳氧鍵「C-O」均勻斷裂,會產生一個「甲基自由基methyl radical」和一個「氫氧自由基OH radical」,並且消耗掉92千卡/莫耳的「鍵解離能」:
5. 我們通常用 「半箭頭half-headed curved arrow」(上圖藍色部分) 來說明一個化學鍵中的1個電子轉移到一個原子身上。
6. 所有化學鍵的均勻斷裂都需要輸入能量來達成,所以整個過程是吸熱的endothermic。
7. 鍵解離能多少?這個問題跟討論鍵長一樣,在不同的分子身上,數值不一樣,舉例如下:
8. 烷類的「碳氫C-H」鍵,鍵長1.10埃,鍵能93-105千卡/莫耳;烷類的「碳碳C-C」鍵,鍵長1.54埃,鍵能84-90千卡/莫耳;胺類的「碳氫C-H」鍵,鍵長1.01埃,鍵能91-103千卡/莫耳;胺類的「碳氮C-N」鍵,鍵長1.47埃,鍵能82-85千卡/莫耳。
註:1埃=10-10次方公尺;1莫耳=6*10 23次方個原子。
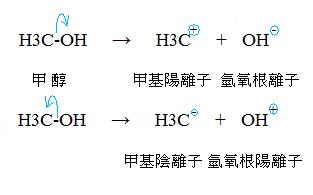
9. 不均勻斷裂Heterolytic cleavage:原本互相鍵結的二個原子,化學鍵被打斷後,電子分配不公平,化學鍵上的二個電子全都被送到其中一個原子。
10. 不均勻斷裂,特別容易發生在有極性的σ鍵(單鍵)身上,因為有極性的化學鍵二端的原子陰電性大小不同,陰電性強的一方在吸引電子的能力上占絕對優勢;不均勻斷裂,比較不會發生在無極性的化學鍵身上。
11. 通常,不均勻斷裂是不容易發生的,因為它需要相當大的能量。要打斷有極性的化學鍵,不僅要打斷σ鍵(單鍵),還要把打斷之後,新產生的正極與負極二方完全拉開,防止它們正負相吸,這真是難上加難。
12. 其實,要讓一個化學鍵有極性,這就已經多添加不少能量在裡面了,因此,在欠缺其他外在因素之下,「不均勻斷裂」所需的能量會多於「均勻斷裂」。
13. 所謂的外在因素,就是讓打斷極性分子的化學鍵時,讓極性分子溶解在極性溶劑裡,來穩定不均勻斷裂後產生的離子;在極性溶劑的幫忙之下,「不均勻斷裂」所需的能量甚至會低於「均勻斷裂」所需的能量。(翻譯改寫自Mary Anne Fox, James K. Whitesell的《Organic Chemistry》)
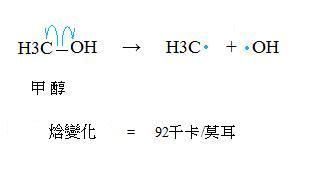
限會員,要發表迴響,請先登入


