1. 計算「碳氫化合物」氧化數的方式,可以同樣類推到包含「異質原子」的有機分子身上。
2. 例如,在催化「亞胺imine」變成「胺amine」的還原反應中,2個氫原子從氫氣狀態的氧化數「0」,變為胺的成員,氧化數增加「+1」;從2個氫原子「被氧化」,我們知道亞胺「被還原」了,亞胺當中的原子氧化數將總共減少「-2」,那麼,到底是哪個原子氧化數少了呢?
3. 亞胺的「氮」與「碳」形成雙鍵時,因為「氮」的負電性較強,所以當「碳-氮」雙鍵中的「氮」,把「碳」的2個電子都搶奪來靠近自己,同時也把「氫」的1個電子搶奪來靠近自己,使得「氮」的氧化數是「-3」;
4. 亞胺催化成胺之後,雖然因為「碳-氮」之間少了一個鍵能,使得「氮」只能從「碳」身上奪走1個電子,但是,「氮」又從新鍵結的「氫」與原本就已經鍵結的「氫」身上,奪走2個電子,結果氧化數是「-3」。也就是亞胺變成胺之後,氮的氧化數一點都沒變。
5. 另一方面,亞胺的「碳」與「氮」與形成雙鍵時,「碳」除了失去2個電子給「氮」之外,「碳」也從2個鍵結的「氫」身上得到2個電子,所以「碳」的氧化數是「0」;
6. 亞胺催化成胺之後,因為「碳-氮」之間少了一個鍵能,使得「碳」只失去1個電子給「氮」,另一方面,卻從3個「氫」身上得到3個電子,總加的結果,「碳」得到2個電子,氧化數是「-2」。
7. 這個決定氧化數的計算方式,也可以類推到有極性的原子身上。例如「胺」和「酸」反應成「胺離子ammonium ions」的反應:「甲基胺methylamine」與「溴化氫HBr」反應成「甲基胺離子Methylammonium」與「溴離子bromide」。
8. 甲基胺離子的骨架是「碳-氫」單鍵,整個反應從頭到尾,「碳」都是和3個「氫」與1個「氮」鍵結,完全沒變,所以「碳」的氧化數不變。
9. 另一方面,甲基胺變成甲基胺離子,雖然「氮」新增加一個與「氫」的化學鍵,應該可以多得1個電子,但是溴離子又從中奪走了1個電子,使得「氮」的氧化數不增不減,沒有氧化,也沒有還原,氧化數保持「-3」不變。
分析推論:
1.Mary Anne Fox, James K. Whitesell在解釋氧化還原反應時,化學式的寫法,仍舊保持在其他章節的慣性,把有機分子當主體、氫氣當插花的配角:
H2氫氣與Pt鉑
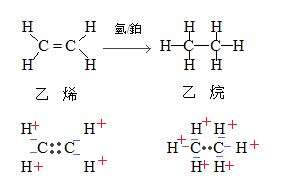
還原反應:C2H4乙烯 →→→→→ C2H6乙烷
2.這會有什麼問題?這種寫法無法清楚地表達「氧化」「還原」的雙重概念,實際上,上述的化學式是「乙烯的還原反應」。
3.而乙烯變成乙烷的「氧化反應」部分,應該是這樣寫的:
C2H4乙烯與Pt鉑
氧化反應:H2氫氣 →→→→→ C2H6乙烷
4.氧化、還原反應是一個「相對共存」的概念,有一方多得電子、還原了,就有一方失去電子、氧化了。多數「化學」教科書描述的時候,都能清楚地點明這種概念,但是「有機化學」教科書,因為太過在意有機分子,而疏忽了氧化、還原的規則。
限會員,要發表迴響,請先登入


